1940 წლის 8 ივნისს აღმოაჩინეს ელემენტი ნეპტუნიუმი. ედვინ მაკმილანმა და ფილიპ ადელსონმა ნეპტუნიუმის სინთეზირება მოახდინეს ურანის ნეიტრონებით დაყომბარებით.

ნეპტუნი პერიოდული სისტემის ქიმიური ელემენტი, ატომური ნომერია 93; აღინიშნება სიმბოლოთი Np.
ნეპტუნიუმი მიეკუთვნება აქტინოიდების ჯგუფს. ის პირველი ტრანსურანული ელემენტია, ის დედამიწაზე არ მოიპოვება და ხელოვნურად იღებენ ურანისგან, ბირთვული რეაქციის საშუალებით.
ნეპტინიუმი არის რადიოაქტიური აქტინიდური ლითონი, ეს ელემენტი ასევე არის პირველი ტრანსურანული ელემენტი. იგი პერიოდულ სისტემაში მდებარეობს ურანის შემდეგ. მისი სახელიც აქედან მოდის, მზის სისტემაში პლანეტა ურანის შემდეგ ნეპტუნი მდეობარეობს.
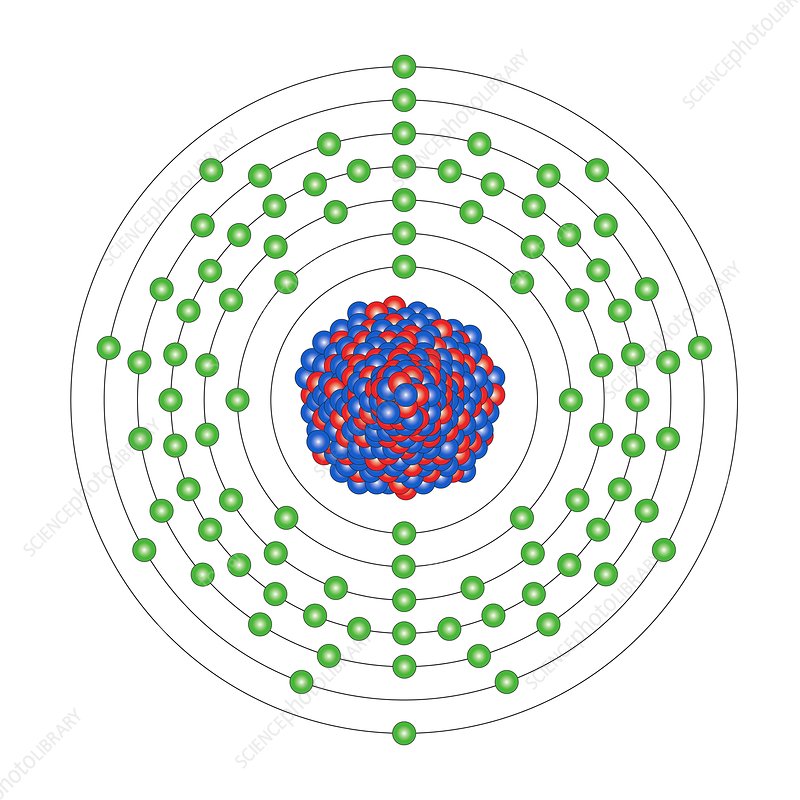
ნეპტუნიუმის ატომს აქვს 93 პროტონი და 93 ელექტრონი, რომელთაგან შვიდი არის ვალენტური ელექტრონი.
ნეპტუნიუმის ლითონი მოვერცხლისფროა. ელემენტი გვხვდება სამი ალოტროპიული ფორმით და ჩვეულებრივ ავლენს ხუთ ჟანგვის მდგომარეობას, +3-დან +7-მდე. ის არის რადიოაქტიური, შხამიანი, პიროფორული ნივთიერება და მისი გამოყენება საშიშია. ორგანიზმში ნეპტუნიუმის იზოტოპების ზღვრული დასაშვები რაოდენობაა: 237Np — 0,06 მკკიური (100 მკგ), 238Np, 239Np — 25 მკკიური (10−4 მკგ).

ელემენტი პირველად სინთეზირებული იქნა ედვინ მაკმილანისა და ფილიპ ჰ. აბელსონის მიერ ბერკლის რადიაციულ ლაბორატორიაში 1940 წლის 8 ივნისს. მას შემდეგ ნეპტუნიუმის მიღება ხდება, ურანის ნეიტრონული დასხივებით ბირთვულ რეაქტორებში.
მიუხედავად იმისა, რომ ნეპტუნიუმს არ აქვს კომერციული გამოყენება, იგი გამოიყენება პლუტონიუმ-238-ის ფორმირებისთვის და რადიოიზოტოპური თერმული გენერატორებისთვის კოსმოსური ხომალდებისთვის ელექტროენერგიის მიწოდებისთვის.
ნეპტუნიუმი ასევე გამოიყენებოდა მაღალი ენერგიის ნეიტრონების დეტექტორებში.
ნეპტუნიუმს იღებენ ნეპტუნიუმის ფტორიდის აღდგენით ბარიუმის ორთქლით 1600 К ტემპერატურაზე:
ნეპტუნიუმის ლითონი ძალიან რეაქტიულია. ნეპტუნიუმის იონები მიდრეკილნი არიან ჰიდროლიზისა და საკოორდინაციო ნაერთების წარმოქმნისკენ.

ნეპტუნიუმი ქიმიურად რეაქტიულია და უფრო ჰგავს პლუტონიუმს, ვიდრე ურანს, ჟანგვის მდგომარეობით +3-დან +7-მდე. ნეპტუნიუმის იონებს წყალხსნარში აქვთ დამახასიათებელი ფერები: Np3+, ღია მეწამული; Np4+, ღია ყვითელი-მწვანე; NpO2+, მწვანე-ლურჯი; NpO22+

გამოყენებული ლიტერატურა:
ელემენტების აღმოჩენები და მათი სახელწოდებების წარმომავლობა
ქიმია და ადამიანი
