თანამედროვე ორგანული ქიმია, შესასწავლი ობიექტების სიმრავლისა და სირთულის მიხედვით, ერთ-ერთი ვრცელი და დინამიკური საბუნებისმეტყველო დისციპლინაა. არსებობს ორგანული ქიმიის რამდენიმე განმარტება. კეკულეს და გმელინის მიხედვით, ორგანული ქიმია ელემენტ ნახშირბადის ქიმიაა, შორლემერის მიხედვით – ნახშირწყალბადებისა და მათი ნაწარმების ქიმია.
XVIII საუკუნეში ნივთიერებებს, წარმომავლობის მიხედვით, ყოფდნენ სამ კლასად: მინერალურ, მცენარეულ და ცხოველურ ნაერთებად.
1807 წელს ბერცელიუსის წინადადებით, ცოცხალი ორგანიზმებიდან მიღებულ ნაერთებს ორგანული ნივთიერებები ეწოდა. ბერცელიუსის მიხედვით – „ორგანული ქიმია სასიცოცხლო ძალების მოქმედების შედეგად წარმოქმნილი ნაერთების ქიმიაა“. ამგვარად, ბერცელიუსი ვიტალისტური თეორიის (სასიცოცხლო ძალები – vis vitalis) მიმდევარი იყო.
ვიტალისტური თეორიის კრახი დაიწყო გერმანელ ქიმიკოს ვიოლერის მიერ განხორციელებული ორი სინთეზით. 1824 წელს მან დიციანის ჰიდროლიზით მიიღო მჟაუნმჟავა:
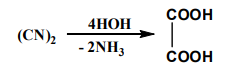
ხოლო 1828 წელა ამინიუმის ოქსიციანიდის გაცხელებით – შარდოვანა:
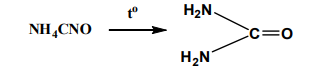
ორგანული ქიმია მეცნიერების ცალკე დარგად გამოიყო ძირითადად სამი მიზეზის გამო:
ტიპიური ორგანული ნაერთები არსებითად განსხვავდება არაორგანულისაგან.
ორგანულ ნაერთთა რიცხვი 20 მილიონს აღემატება, მაშინ, როდესაც არაორგანულ ნივთიერებათა რიცხვი ნახევარ მილიონამდეა;
ორგანული ნაერთები განსაკუთრებულ როლს ასრულებენ სასიცოცხლო პროცესებში. ორგანული ქიმიის ისტორიაპირობითად შეიძლება დაიყოს შემდეგ პერიოდებად:
ა) ე მ პ ი რ უ ლ ი პერიოდი – ორგანულ ნაერთებთან ადამიანის პირველი ნაცნობობიდან ორგანული ქიმიის, როგორც მეცნიერების ჩამოყალიბებამდე (XVIII საუკუნის ბოლო პერიოდებში);
ბ) ა ნ ა ლ ი ზ უ რ ი პერიოდი – XVIII საუკუნის ბოლოდან XIX საუკუნის 60-იან წლებამდე;
გ) ს ტ რ უ ქ ტ უ რ უ ლ ი პერიოდი – XIX საუკუნის 60-იანი წლებიდან XX საუკუნის ათიან წლებამდე;
დ) ფ ი ზ ი კ ა ლ ი ზ ა ც ი ი ს პერიოდი – XX საუკუნის ათიანი წლებიდან XX საუკუნის ბოლომდე. დღეისათვის ორგანული ქიმია შევიდა განვითარების ახალ პერიოდში – კ ი ბ ე რ ნ ე ტ ი კ უ ლ პერიოდში, რაც გულისხმობს პროგრამირებისა და კომპიუტერული ტექნიკის ფართოდ დანერგვას როგორც ქიმიურ ტექნოლოგიებში, ისევე აკადემიური ხასიათის კვლევა-ძიებებში. (ამის დასტურია თეორიული ქიმიის ახალი დარგების – კომპიუტერული ქიმიისა და მათემატიკუფრი ქიმიის ჩამოყალიბება).
კეკულემ დაადგინა, რომ ნახშირბადი ყველა ორგანულ ნაერთში ოთხვალენტიანია. გარდა ამისა, მან აჩვენა, რომ ნახშირბადატომებს უნარი აქვთ წარმოქმნან სხვადასხვა სიგრძისა და კონფიგურაციის ნახშირბადოვანი ჯაჭვები. კეკულემ მოგვაწოდა ბენზოლის ციკლური ფორმულაც. აღსანიშნავია შოტლანდიელი ქიმიკოსის კუპერის როლიც. მან შემოიტანა სტრუქტურულ ფორმულებში ხაზაკის (-) გამოყენება.
აღნაგობის თეორიის არსი ფორმულირდება ოთხი ძირითადი დებულების სახით:
მოლეკულებში ატომები ერთმანეთთან დაკავშირებულია მკაცრად განსაზღვრული თანმიმდევრობით ე.ი. თითოეულ ნაერთს გააჩნია მისთვის დამახასიათებელი მოლეკულური აღნაგობა, ანუ სტრუქტურა. არსებობს ზუსტი კანონზომიერება ატომების ურთიერთშეკავშირების მიმდევრობასა და თავისებურებებს შორის, რომელიც დამახასიათებელია თითოეული კონკრეტული ნაერთისათვის.
ნივთიერების თვისებები დამოკიდებულია მის მოლეკულებში შემავალი ატომების ტიპზე, რიცხვზე და ერთმანეთთან დაკავშირების თანმიმდევრობაზე.
ნივთიერების აღნაგობა შეიძლება დადგინდეს ქიმიური გარდაქმნების შესწავლის შედეგად და, პირიქით, ნივთიერების აღნაგობის საფუძველზე შეიძლება განისაზღვროს მისი თვისებები.
ურთიერთგავლენას ახდენენ როგორც ერთმანეთთან უშუალოდ დაკავშირებული, აგრეთვე სხვა ატომების საშუალებით ბმული ატომები. ანუ, თვისებები ხარისხობრივად იცვლება იმის მიხედვით, თუ რომელი ატომები რომელ ატომებთან და როგორ არიან დაკავშირებული. კონკრეტული ნივთიერების მოლეკულის ჭეშმარიტი აღნაგობა შეიძლება გამოისახოს გარკვეული ფორმულით და ეს ფორმულა ერთადერთია მოცემული ნაერთისათვის.
მიუხედავად იმისა, რომ აღნაგობის თეორიის საფუძვლების ჩამოყალიბებიდან საუკუნენახევარია გასული, იგი დღესაც რჩება ქიმიკოს-ორგანიკოსის მეგზურად. ბრწყინვალე ამერიკელი ქიმიკოს-ორგანიკოსის რობერტ ვუდვორდის სიტყვებით: „აღნაგობის თეორია ორგანულ ქიმიაში მომხდარი პირველი დიდი რევოლუციაა“.
ამ მოძღვრების თანამედროვე ვარიანტი (ე.წ. მოლეკულური მექანიკა) წარმოადგენს თეორიული ორგანული ქიმიის დამოუკიდებელ და ინტენსიურად განვითარებად ნაწილს, რომელიც კვანტური წარმოდგენების პარალელურად, მნიშვნელოვან როლს ასრულებს მოლეკულათა აღნაგობისა და რეაქციის უნარიანობის თეორიულად შესწავლის საქმეში.
აღნაგობის თეორიის ფარგლებში შესაძლებელი გახდა იზომერიის მოვლენის წინასწარმეტყველება და თეორიული ინტერპრეტაცია. ტრადიციულად, განმარტების მიხედვით, იზომერები ეწოდებათ ნივთიერებებს, რომელთაც აქვთ ერთნაირი თვისობრივი და რაოდენობრივი შედგენილობა (ერთნაირი მოლეკულური ფორმულა), მაგრამ სხვადასხვაგვარი აღნაგობა და,
აქედან გამომდინარე, სხვადასხვა თვისებები. დღეისათვის აღმოჩენილია იზომერთა ისეთი ტიპებიც, რომლებიც ძალზე არასტაბილურნი არიან და დროის მოკლე ინტერვალში განიცდიან ურთიერთგადასვლას. ამგვარად, ინდივიდუალური იზომერების დაფიქსირების შესაძლებლობას განსაზღვრავს ის, თუ გამოყენებულ ექსპერიმენტულ მეთოდში დროის როგორ ინტერვალში წარმოებს გაზომვა. აქედან გამომდინარე, შეიცვალა იზომერის ცნების განმარტებაც. რუვრის
თანამედროვე ინტერპრეტაციით, ი ზ ო მ ე რ ე ბ ი ეწოდებათ იდენტური მოლეკულური ფორმულის მქონე ინდივიდუალურ ქიმიურ ნაერთებს, რომლებსაც განსხვავებული აქვთ ესა თუ ის ფიზიკურ-ქიმიური თვისება და რომლებიც სტაბილურნი არიან დროის უფრო ხანგრძლივ ინტერვალში, ვიდრე მათი შესასწავლი თვისების გაზომვისთვისაა საჭირო.
და ბოლოს, მკაფიოდ განვსაზღვროთ ცნების – „სხვადასხვა ტიპის ფორმულის“ ცნების არსი ორგანულ ქიმიაში.
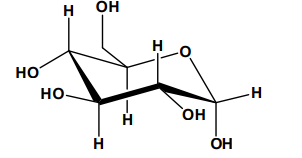
გლუკოზის მაგალითზე განვიხილოთ სხვადასხვა სახის ფორმულების სახელწოდება. მოლეკულური ფორმულა – C6H12O6 გვიჩვენებს, რომ ამ ნაერთის მოლეკულა შეიცავს 6 ნახშირბადატომს, 12 წყალბადატომს და 6 ჟანგბადატომს. ამგვარად, მოლეკუკური ფორმულა ასახავს ნაერთის თვისობრივ და რაოდენობრივ შედგენილობას.
სტრუქტურული ფორმულა გვიჩვენებს მოლეკულაში ატომების შეერთების წესს, ანუ თანმიმდევრობას და მათ შორის ბმების რიგს. გლუკოზის სტრუქტურული ფორმულაა:
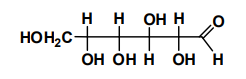
ხშირად გამოიყენება ე.წ. შეკვეცილი სტრუქტურული ფორმულა:
CH2OH – CHOH – CHOH – CHOH – CHOH – CHO
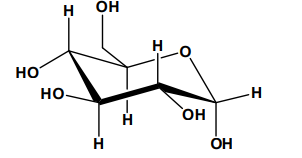
გამოსახულებას, რომელიც გვიჩვენებს მოლეკულის სივრცით აღნაგობას სტერეოფორმულა (სივრცითი ფორმულა) ეწოდება:
ავტორი:
ლია კვირიკაძე